Investor
Relations
BIONEER is a new-paradigm healthcare company, providing
total-solution across Disease prevention, Diagnosis, and Treatment
BIONEER is a new-paradigm healthcare company, providing
total-solution across Disease prevention, Diagnosis, and Treatment

Why Invest in
 ?
?
- Pipelines
- All-in-House
- Ecosystem
- CapEx
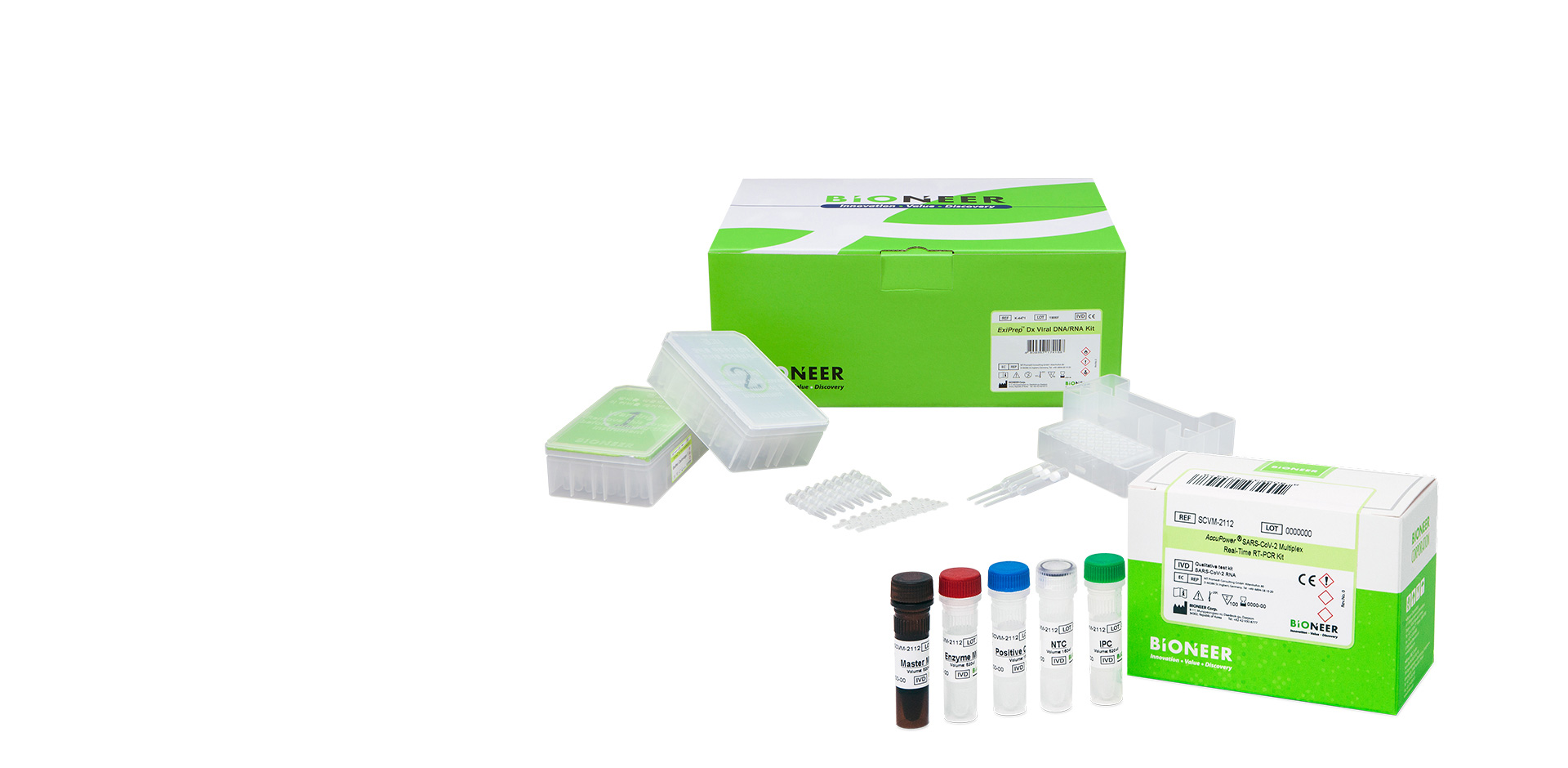
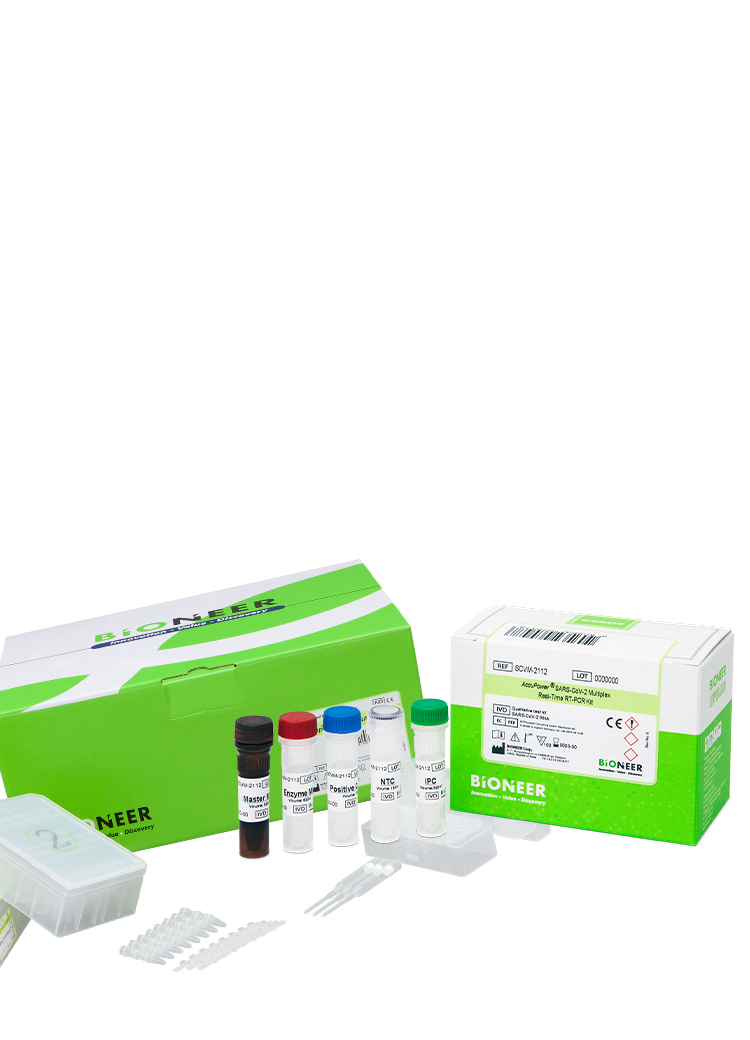
All-in-House
BIONEER All-in-House system from R&D to production
ensures high sensitivity & specificity of MDx products


MDx Ecosystem
BIONEER Ecosystem enables customization
for each customer with its varied product portfolio
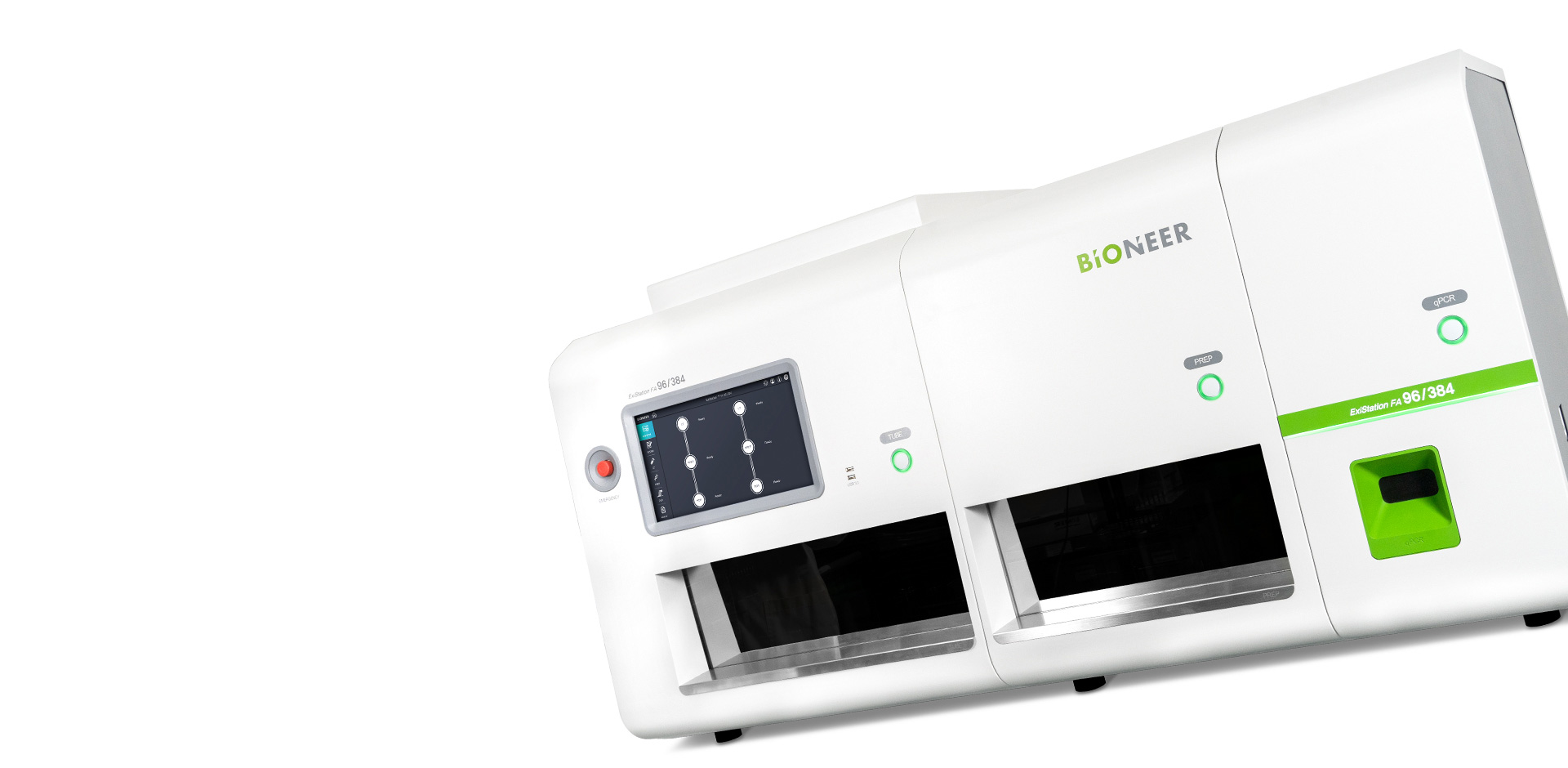

CapEx
BIONEER increased its production capacity
to maximize revenue with expansion of Global MDx Center
BIONEER increased its production capacity
to maximize revenue with expansion of Global MDx Center

Healthier Future for Humanity with solutions
across Disease Prevention-Diagnosis-Treatment
BIONEER was established as the first Korean biotechnology company in 1992.
Since then, we worked toward the goal of contributing to human health
with its total-care platform for disease prevention, diagnosis, and treatment.
Moving forward as a global healthcare company, BIONEER will
continuously take initiatives and pursue innovation to achieve our mission.
Healthier Future for Humanity with solutions
across Disease Prevention-Diagnosis-Treatment
BIONEER was established as the first Korean biotechnology company in 1992.
Since then, we worked toward the goal of contributing to human health
with its total-care platform for disease prevention, diagnosis, and treatment.
Moving forward as a global healthcare company, BIONEER will
continuously take initiatives and pursue innovation to achieve our mission.




